
财联社10月15日讯(记者 卢阿峰) 创新药“一哥”推动卡瑞利珠单抗在美上市的决心非常坚定,距离收到CRL导致第一次上市申请失败仅过去五个月,恒瑞医药(600276.SH)再度提交了卡瑞利珠单抗在美上市的申请。
恒瑞医药今日晚间发布公告,公司收到美国食品药品监督管理局(以下简称“FDA”)的《确认函》,公司重新提交的注射用卡瑞利珠单抗联合甲磺酸阿帕替尼片用于不可切除或转移性肝细胞癌患者的一线治疗的生物制品许可申请(BLA)获得FDA受理。
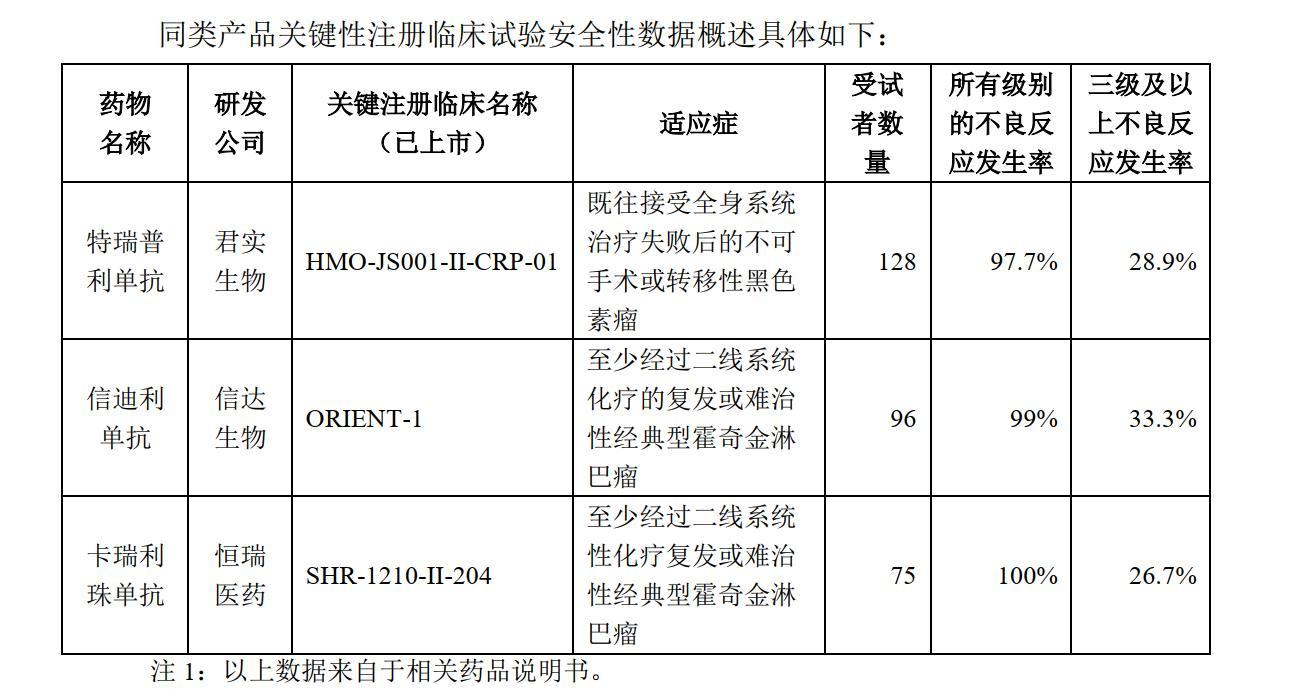
有业内专家告诉财联社记者,恒瑞医药的卡瑞利珠单抗在美上市过程似乎有复刻君实生物的特瑞普利单抗的迹象,“如果卡瑞利珠单抗能在美成功上市,恒瑞医药国际化发展将迈上一个新台阶。”
此前曾遭遇程序延迟
这是恒瑞医药第二次在美提交卡瑞利珠单抗在美上市申请,第一次提交并获得受理的时间是2023年7月。但在2024年5月,卡瑞利珠单抗肝癌联合疗法的大中华区和韩国以外的全球开发和商业化独家授权方Elevar Therapeutics的母公司HLB-LS收到了FDA就卡瑞利珠单抗联合阿帕替尼用于一线治疗不可切除肝细胞癌患者的新药申请(NDA)发出的完整回复函(CRL)。

FDA在CRL中主要强调了两项内容:一是化学、制造和控制(CMC)问题;二是FDA对在俄罗斯和乌克兰的关键临床试验中心的检查尚未完成。这意味着恒瑞PD-1组合疗法在美国上市的程序延迟。
有业内专家告诉财联社记者,CRL相当于提出了需要整改的地方或措施,另一方面说明该疗法研发已经比较规范,接近或者达到了相关要求,理论上来说,恒瑞在规定时间内完成整改后就可以重新提出上市申请。
资深医药行业专家杨涛今日对财联社记者表示,美国新药注册领域的政治因素考量很少,特别是单抗这些技术比较成熟的产品类别,中国和印度企业在过去被查出问题的都不少,“美国FDA故意刁难没有太大的意义。”

会复刻君实PD-1在美上市路径?
财联社记者注意到,君实生物-U(688180.SH)的PD-1产品也曾在美国申请上市的过程中收到过CRL。
公开信息显示,2022年5月,君实生物的特瑞普利单抗上市申请收到FDA的CRL,FDA要求进行一项质控流程的变更,君实生物认为这一变更较容易实施。2022年7月,君实生物重新提交了特瑞普利单抗的上市申请并获FDA受理,最终在2023年10月获得FDA正式批准上市。
对于恒瑞医药在美的上市过程,似乎正在复刻君实生物的特瑞普利单抗的获批过程,有业内专家对财联社记者表示,“确实有点像,就看结果会怎么样。”
但杨涛表示两者还有一点区别,“确实可以复刻,但字面上看恒瑞医药的缺陷相比君实生物的难改。”
值得注意的是,恒瑞医药除了上述CRL,在今年6月还收到了美FDA发出的检查常见文件483表格。恒瑞医药方面表示,此次收到的483表格涉及的不是卡瑞利珠单抗、阿帕替尼组合申请所涉及的生产场地,公司出口美国制剂未受影响。
杨涛对财联社记者表示,卡瑞利珠单抗虽然在国内获批了多项适应症,但国内市场和国际市场的体量差异显而易见,若是其PD-1品种在美获批,恒瑞医药的国际化发展战略可谓迈上了一个台阶。
恒瑞医药同时也在公告中提示,国外有多款PD-1单克隆抗体获批上市,包括帕博利珠单抗(默沙东)、dostarlimab(葛兰素史克)等,国内也有多款同类产品获批上市,2023年抗PD-1抗体全球销售额合计约为375.92亿美元。由于FDA现场核查的时间及结果存在不确定性,本次BLA能否获得批准存在不确定性。
恒瑞医药卡瑞利珠单抗拟纳入突破性治疗,pd-1抑制剂「销冠」品种
恒瑞医药的卡瑞利珠单抗在免疫治疗领域取得重要突破,被纳入国家药品监督管理局突破性治疗品种名单,适用于PD-L1阳性且无EGFR/ALK基因异常的复发性或转移性非小细胞肺癌的一线治疗。 这款药物凭借其卓越的市场表现,曾在国内PD-1抑制剂市场中脱颖而出,2020年销售额达到新高,但在医保政策影响下,2022年上半年的增长速度有所放缓。 2018年以来,国产PD-1抑制剂市场迅速扩大,卡瑞利珠单抗凭借首当其冲的医保定价,从高价变为亲民药物,价格大幅下降后,虽然销量激增,但对公司抗肿瘤业务营收产生一定影响。 然而,恒瑞医药并未止步,卡瑞利珠单抗已获批多个适应症,覆盖肺癌、肝癌等多瘤种,且正通过与其他公司的合作和在更多癌种的临床研究,寻求市场拓展的新路径。 尽管面临竞争激烈的市场环境,恒瑞医药通过多元化布局,持续推动卡瑞利珠单抗的临床研发,显示了其对未来市场动态的敏感性和应对策略。 这一系列举措表明,卡瑞利珠单抗虽然在增速上有所放缓,但在创新和市场适应性上仍然具备潜力。
艾瑞卡PD-1免疫治疗药可以治疗肺癌吗?有效果吗?
艾瑞卡也叫卡瑞利珠单抗,它是恒瑞肿瘤自主研发并具有知识产权的人源化PD-1单克隆抗体药物,能够与人PD-1受体结合,阻断PD-1/PD-L1通路,达到恢复机体的抗肿瘤免疫力的效果,建立癌症免疫治疗基础,在肺癌、肝癌、食管癌、鼻咽癌以及淋巴瘤五大瘤种中获批了8个适应症,有相关需要的可以具体去官网了解下。

恒瑞医药有哪些具有全球或中国首个创新性的产品?
恒瑞医药有多个上市产品开创“全球首个”“中国首个”的创新性,如卡瑞利珠单抗(艾瑞卡®)联合阿帕替尼(艾坦®)(“双艾”)是全球首个获批的用于治疗晚期肝细胞癌的PD-1抑制剂与小分子抗血管生成药物的组合,瑞维鲁胺(艾瑞恩®)是中国首个自主研发的新型雄激素受体(AR)抑制剂,阿得贝利单抗(艾瑞利®)是中国首个获批小细胞肺癌适应症的自主研发PD-L1抑制剂。





